
پیوند شیمیایی چیست با انواع آن بیشتر آشنا شوید
همه ی ما میدانیم که مواد از اتم ها و مولکول ها ساخته شده اند .برای همین منظور باید بین اتم ها یا مولکول ها پیوند هایی برقرار شود تا در کنار هم قرار بگیرند و مواد مختلف را بسازند.به این پیوند ها پیوند های شیمیایی گفته میشود.معروف ترین پیوند های موجود پیوند کوالانسی پیوند یونی و پیوند هیدروژنی هستند. پیوند شیمیایی که ناشی از ترکیب شدن اتمها هستند درواقع از تغییر آرایش الکترونی حاصل میشوند.
پیوندهای شیمیایی و انواع آن:
1. پیوند فلزی :
این پیوندها در فلزات و آلیاژها دیده میشود. اتمها در ساختاری سهبعدی قرار دارند و الکترونهای لایهای بیرونی این اتمها آزادانه در سراسر این ساختار حرکت میکنند و وظیفه به هم نگهداشتن لایه مزبور را به عهده دارد.
ساختار سهبعدی پیوندهای فلزی را به مانند ظرفی مملو از چسب در نظر بگیرید که گویهایی در آن جای گرفتهاند. با ذرات چسب مایع که به هم پیوسته و در سراسر ظرف پراکندهاند به منزله الکترونهای آزاد و گویها در نقش اتم میباشد.
پیوند یونی
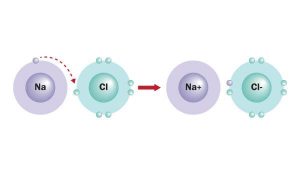
از دیگر پیوند شیمایی پیوندی که بین دو اتم با بار مخالف ایجاد می شود پیوندی یونی است. یک نیروی جاذبه الکترواستاتیکی بسیار قوی است که از انتقال الکترون از یک اتم فلزی به اتمی نافلز ایجاد می شود. به عنوان مثال سدیم که در گروه یک جدول تناوبی است یک الکترون خود را از دست می دهد و به Na+ تبدیل می شود و کلرید که در گروه هفدهم جدول تناوبی است یک الکترون می گیرد و به Cl– تبدیل می شود. به علت وجود بار مثبت و منفی، دو اتم کنار هم قرار می گیرند و پیوندی بسیار قوی تشکیل می دهند.
شرایط تشکیل پیوند یونی:
- اتم تشکیل دهنده کاتیون انرژی یونیزاسیون کمی داشته باشد.
- اتم تشکیل دهنده آنیون آنتالپی بالایی برای دربافت الکترون داشته باشد.
- آنتالپی بالایی در شبکه منفی کریستال تشکیل شده داشته باشد.
خواص و ویژگی های پیوندهای یونی
- ترکیبات یونی مذاب وقتی در میدان الکتریکی قرار می گیرند، یون هایشان آزادانه حرکت می کنند و می توانند رسانای الکتریکی باشند. اگر به صورت جامد باشند یون ها نمی توانند حرکت کنند و در نتیجه خاصیت رسانایی ندارند.
- این ترکیبات به علت نوع پیوندشان بسیار پایدار هستند و سختی بالایی دارند.
- به علت آرایش منظمی که دارند بسیار شکننده اند. به عنوان مثال نمک سدیم کلرید آرایشی شش وجهی دارد. اگر یکی از سطوح یونی آن جابجا
- شود، یون های با بار یکسان در مقابل هم قرار می گیرند و یکدیگر را دفع می کنند و در نتیجه بلور می شکند.
پیوند کووالانسی
وقتی اتم ها به جای انتقال الکترون ، الکترون به اشتراک بگذارند پیوند کووالانسی ایجاد میشود.در دنیای زنده از جمله بدن ما پیوند کووالانسی از یونی معمول تر است.اگر اتم ها هر کدام یک الکترون به اشتراک بگذارند پیوند یگانه ؛ اگر دو الکترون به اشتراک بگذارند پیوند دوگانه و اگر هر کدام سه الکترون به اشتراک بگذارند پیوند سه گانه ایجاد می شود.
در پیوند کووالانسی لایه های ابری درون هم فرو میروند مثلا در تشکیل مولکول آب دو اتم هیدروژن و یک اتم اکسیژن با هم پیوند کووالانسی تشکیل میدهند . اتم هیدروژن کلا یک الکترون دارد و اتم اکسیژن در لایه ظرفیت خود دو الکترون دارد . اتم اکسیژن هر کدام از الکترون هایش را با یک هیدروژن به اشتراک گذاشته و در نهایت بین اکسیژن و هیدروژن ها پیوند های کووالانسی ایجاد میشود. وقتی میگویم اشتراک گذاری الکترون یعنی الکترون علاوه بر این که ; مدتی در لایه ابری اتم خود قرار دارد مدت زمانی را نیز در لایه ابری اتم مجاور می گذراند ؛ یعنی بین این لایه و آن لایه در رفت و آمد است. پیوند های کووالانسی بر دو نوع اند: قطبی و غیرقطبی
پیوندها با نیروی واندروالسی:
به طور کلی نیروی جاذبهای که در مولکولهای قطبی، قطبی قطبی، نا قطبی نا قطبی، نا قطبی وجود دارد نیروی واندروالسی میباشد.
پیوند هیدروژنی
اتم هیدروژنی معمولا کمترین الکترونگاتیوی را دارد وقتی با اتمی پیوند کووالانسی قطبی تشکیل میدهد اتم هیدروژن دارای بار جزئی مثبت میشود . حال اگر اتمی با بار جزئی منفی به این اتم هیدروژن نزدیک شود یک نیروی جاذبه بین این دو برقرار میشود و منجر به تشکیل پیوند هیدروژنی میشود.در طبیعت پیوند هیدروژنی بسیار معمول است . مثل آب یا ترکیبات آلی .
پیوند داتیو:
نوعی پیوند کوالانسی است که دران جفت الکترون پیوندی توسط یکی از اتمها به اشتراک گذاشتهشده و اتم دیگر جفت الکترون را میپذیرد.
پیوند داتیو در نحوهی تشکیل با پیوند کوالانسی معمولی تفاوت دارد.
پیوند موجود در مولکول از نوع داتیو است.
شرط تشکیل پیوند داتیو: پیوند داتیو در حالتی تشکیل میشود که یک اتم (در مولکولها به عنوان اتم مرکزی) دارای حداقل یک جفت الکترون ناپیوندی در لایه بیرونی خود بوده و اتمی دیگر (در مولکولها به عنوان اتم مرکزی) حداقل یک اوربیتال خالی در لایه بیرونی خود داشته باشد.


