
حلال و حل شونده چیست؟ نحوه تشکیل محلول ها
حلال و حل شونده
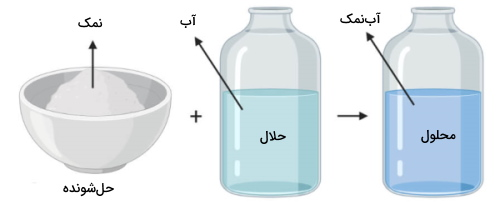
حلال و حل شونده را میتوان اینگونه بیان کرد در یک محلول به جزء با مقدار بیشتر، حلال و به جزء با مقدار کمتر، حلشونده میگویند و این ماده به شکلی یکنواخت (همگن) در حلال توزیع (حل) شده است. بر اساس این تعریف، در یک محلول، تنها یک ماده شیمیایی را میتوان به عنوان حلال در نظر گرفت. بنابراین، اگر تنها دو ماده شیمیایی در یک محلول وجود داشته باشند، یکی حلال و دیگری حلشونده خواهد بود. اگر یک محلول شامل ۳ یا چند ماده شیمیایی باشد، یک ماده را باید به عنوان حلال مشخص کرد و مابقی مواد نیز حلشونده خواهند بود. رفتارهای کمی و سنجشهای کیفی یک محلول به حلال و حل شونده موجود در یک محلول بستگی دارند. بنابراین، برای فهم و بکارگیری مفاهیم مرتبط با محلولها در شیمی، هر ماده موجود در محلول را باید در ابتدا به حلال و حل شونده تقسیم کرد.
حلال چیست؟
اصطلاح حلال به دسته ای از ترکیبات شیمیایی اطلاق می شود که به معنای سست کننده پیوند است . در شیمی ، از حلال ها – که عموماً به صورت مایع هستند – برای حل کردن ، تعلیق یا استخراج مواد دیگر استفاده می شود بدون اینکه تغییر شیمیایی در محلول یا مواد دیگر ایجاد کند. از حلال های مختلف در طیف گسترده ای از کاربردهای روزمره استفاده می شود – از رنگ و محصولات مراقبت شخصی و دارویی گرفته تا سموم دفع آفات ، مواد پاک کننده و جوهر. بدون حلال ، بسیاری از محصولات مورد اعتماد ما عملکرد خوبی نخواهند داشت. حلال ها بسیار متنوع هستند و نیازهای خاص تولید محصولاتی با ویژگی های عملکردی مطلوب را برآورده می کنند ، از جمله رنگ های اسپری که به سرعت خشک می شوند و نازل اسپری را مسدود نمی کنند ، جوهرهایی که لک تیره ایجاد نمی کنند، رنگ هایی که به نظر خوب می آیند و مدت طولانی دوام دارند و پاک کننده هایی که برای مشاغل سخت و چرب مناسب هستند.
نحوه تشکیل محلول ها
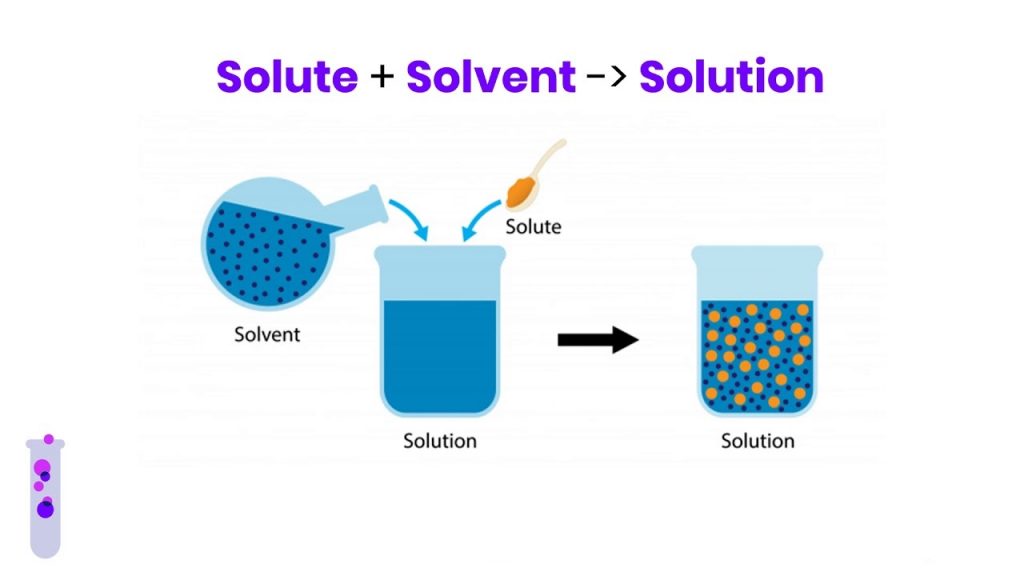
یک محلول زمانی شکل میگیرد که مادهای در ماده دیگری حل شود و دیدیم که مادهای که با مقدار کمتر وجود دارد، حلشونده نام دارد که در حلال، حل میشود. در مثالی دیگر، اگر دو فلز مس و قلع را ذوب و در یکدیگر حل کنیم، نوعی محلول به نام برنز بدست میآید که به آلیاژ برنز معروف است. از آنجایی برنز، بیشتر از مس تشکیل شده است، مس را حلال و قلع را حلشونده مینامیم. همانطور که گفتیم، این دو فلز در حالت مذاب با یکدیگر مخلوط شدند اما در دمای اتاق، محلولی جامد خواهیم داشت.
حقایقی در رابطه با حل شونده ها
حل شونده معمولاً یک جامد است که در مایع حل می شود. یک نمونه روزمره حل شدن نمک در آب است. نمک ماده ای است که در آب به عنوان حلال حل می شود و یک محلول نمکی تشکیل می دهد. از طرف دیگر بخار آب به عنوان یک ماده حل شونده در هوا در نظر گرفته می شود زیرا نیتروژن و اکسیژن در غلظت های بسیار بیشتری در هوا وجود دارند. غلظت یک حل شونده برابر با مقدار حل شونده تقسیم بر حجم کل محلول است. یک حلال می تواند مقادیر مختلفی از حل شونده را رقیق کند که بستگی به میزان استفاده از یک حلال و تفکیک راحت مولکول های حل شونده دارد. این ویژگی حل شونده برای حل شدن در یک حلال به عنوان قابلیت انحلال شناخته می شود. عامل مهمی که در حل شدن سریع حل شونده موثر است سطح در معرض آن است. به عنوان مثال در صورت استفاده از نمک درشت ، سطح کمتری در معرض آب قرار می گیرد و حل شدن همان مقدار نمک بیشتر از نمک ریز طول می کشد. نمک ریزتر باعث می شود که یون های بیشتری در معرض آب قرار بگیرند و حل شونده سریعتر در آب پخش می شود و در نهایت دیگر نمکی در کف لیوان دیده نمی شود زیرا به طور مساوی در سراسر لیوان پخش خواهد شد.
انواع حلال ها
طبقه بندی شیمیایی یک حلال بر اساس ساختار شیمیایی آن است. به عنوان مثال حلال های هیدروکربنی بر اساس نوع “اسکلت کربن” مولکولهایشان در سه زیر گروه طبقه بندی می شوند و به ما خانواده حلال های آلیفاتیک ، آروماتیک و پارافینی را می دهند. رقیق کننده رنگ نمونه متداول حلال هیدروکربنی است. حلال های اکسیژنه از طریق واکنش های شیمیایی الفین ها (حاصل از روغن یا گاز طبیعی) تولید می شوند و به ما الکل ها ، کتون ها ، استرها ، اترها ، گلیکول اترها و استرهای گلیکول اتر را می دهند. حلال های هالوژنه حلال هایی هستند که حاوی هالوژن مانند کلر ، برم یا ید هستند. بسیاری از افراد پرکلرواتیلن را به عنوان نمونه – حلال بسیار موثری که در خشکشویی استفاده می شود – می شناسند.
انواع حل شونده
حل شونده ها می توانند یونی یا کوالانسی باشند. حل شونده های یونی هنگام حل شدن به یون های مجزا تفکیک می شوند درحالیکه حل شونده های کووالانسی به مولکول های مجزا تفکیک می شوند. مثلا نمک طعام (سدیم کلرید) یک حل شونده یونی است. یون های مثبت سدیم جذب سر منفی مولکول های آب شده و یون های منفی کلر جذب سر مثبت مولکول آب که هیدروژن است می شوند. از طرف دیگر شکر یک ترکیب کووالانسی است و موقع حل شدن در آب مولکول های مجزای گلوکز را تشکیل می دهد. جالب است بدانید شکر مانند آب یک ترکیب قطبی و دارای دو سر مثبت و منفی است نیروهای جاذبه بین بارهای مخالف بین مولکول های آب و شکر سرانجام تمام بلورهای شکر را از هم تفکیک کرده و توسط مولکول های آب احاطه می شوند.


